Le cours de chimie des surfaces et colloïdes est réparti en trois chapitres. Chaque chapitre se limite à l’exposé des acquisitions de base, et nous avons enrichit chaque chapitre avec des vidéos qui aident l'étudiant à comprendre.
Le premier chapitre (tensioactivité) traite la notion de la tension superficielle. Nous reconnaissons le concept de force qui découle du déséquilibre des forces qui inflencent les molécules situées à l’interface. la tension superficielle est un phénomène physico-chimique lié aux interactions moléculaires d'un liquide. Le système tend vers un équilibre correspondant à la configuration de plus basse énergie, il modifie donc sa géométrie pour diminuer l'aire de cette interface. La force qui maintient le système dans cette configuration est la tension superficielle.
A température élevée le corps se dilate, les forces d'interactions mutuelles entre les molécules internes et celles de la surface diminuent. Dans ce cas la surface ou l'interface devient moins cohérente et plus fragile d’où la diminution de la tension superficielle.
Il existe différentes méthodes permettant d'aboutir à une valeur de la tension superficielle, Ces dernières ne sont pas toutes égales en terme de précision ou de rapidité. Nous verrons ainsi en première partie que la capillarité permet aussi de déterminer la tension superficielle. Une autre méthode recommandée exigeant une manipulation plus importante ; appelée méthode d'arrachement. Enfin la méthode de la goutte pendante ou stalagmomètre qui demande une manipulation à beaucoup de calculs.
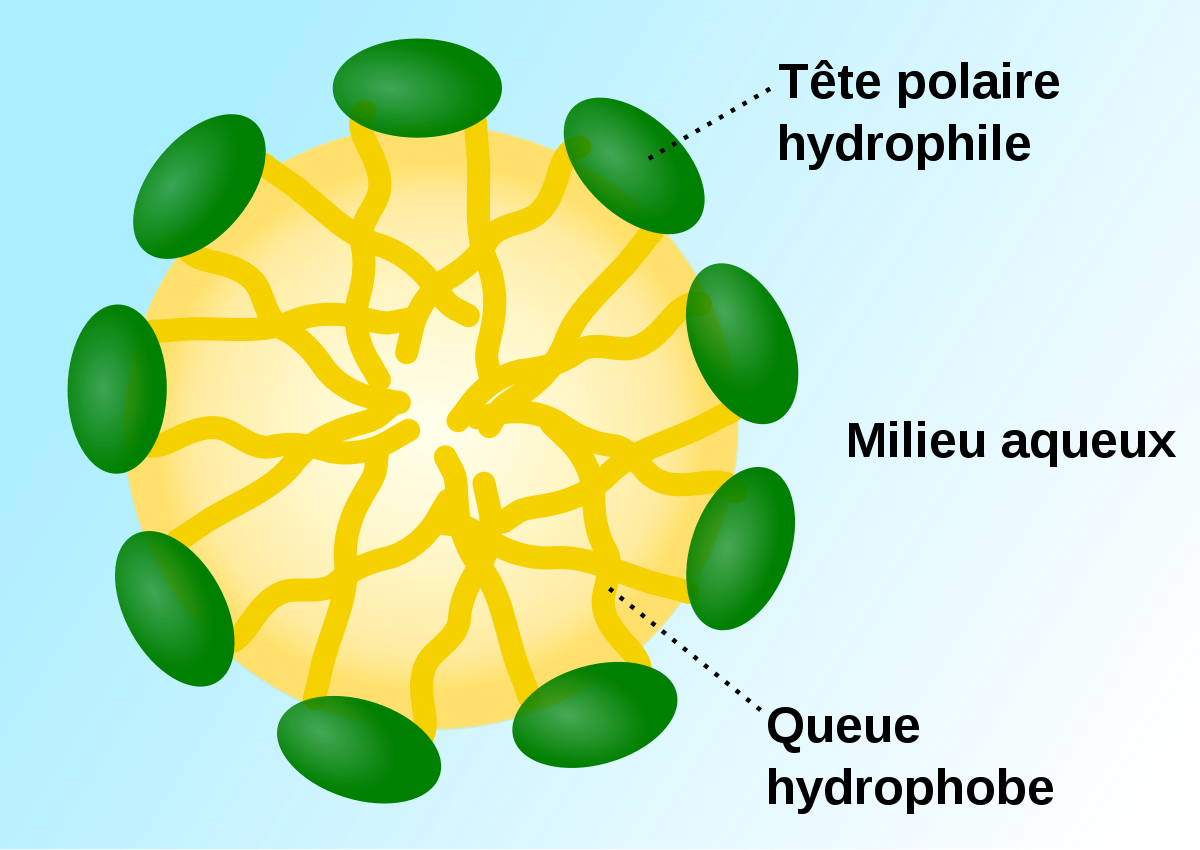
Le deuxième chapitre (Physico- chimie des surfaces), il porte sur l’étude détaillée de la physico-chimie de la tensioactivité. Nous commençons par le travail d’adhésion étant fourni pour séparer deux milieux collés . En définissant le coefficient d’étalement et l’ angle de contact , nous pouvons déterminer les types de mouillage du liquide la surface d’un substrat . De nouvelles molécules apparaissent, appèlées les tensionactifs. Ces agents tensioactifs abaissent la valeur de la tension superficielle des liquides où ils se trouvent pour les rendre mouillants, moussants, détergents, émulsifiants...
Le troisième chapitre (Adsorption des liquides) est consacré à l’étude de la tension de surface des solutions aqueuses. L'adsorption est dite positive si la concentration en surface est supérieure à la Concentration en profondeur l’adsorption. D’une manière très simple, la relation de Gibbs- Duhem est établie pour nous informer que la quantité de soluté adsorbée dépend explicitement de la pente (d γ/dC); Ceci veut dire que si la tension superficielle n’évolue plus avec la concentration du soluté, cette loi peut être appliquée pour déterminer l'aire et le poids moléculaires.
- Teacher: bouazza fatma